Vol. 4, N° e642,
año 2022
Vol. 4, N° e642,
año 2022
ISSN – Online: 2708-3039
DOI:
https://doi.org/10.47796/ing.v4i0.642
![]()
Artículo
original
Caracterización de
nanopartículas de óxido de zinc procedente de pilas carbono zinc sintetizadas
por electrólisis alcalina
Characterization
of zinc oxide nanoparticles from carbon zinc batteries synthesized by alkaline
electrolysis
Felipe Maquera Llica[1]
![]() https://orcid.org/ 0000-0001-7777-7617
https://orcid.org/ 0000-0001-7777-7617
Williams Sergio Almanza Quispe[2]
![]() https://orcid.org/
0000-0003-4453-3610
https://orcid.org/
0000-0003-4453-3610
Agapito Flores Justo[3]
![]() https://orcid.org/
0000-0002-4580-5799
https://orcid.org/
0000-0002-4580-5799
Recibido: 20/07/2022
Aceptado: 30/09/2022
Publicado: 12/10/2022
Resumen
Las pilas y baterías son dispositivos donde
la energía química se transforma en eléctrica. Al ser desechadas pueden contaminar
el ambiente, su contenido de zinc en forma pura y en forma de óxidos representa
un porcentaje importante del peso del total. Con la finalidad de aprovechar las
pilas carbono zinc, se recuperó las nanopartículas de óxido de zinc mediante el
método de electrólisis alcalina y se caracterizó con el propósito de conocer
sus características estructurales mediante la microscopía electrónica de
barrido (SEM). La distribución de las partículas es variable en la escala de
500 nm que muestra conglomerados cristalinos constituidos por partículas más
pequeñas y alargados entre 66 y 115 nm que distan de una simetría hexagonal
característica tipo wursita, no obstante, el patrón de difracción de rayos X es
similar al patrón estándar para óxido de zinc. Estas nanoparticulas pueden ser
empleadas por su mayor energía y área superficial en múltiples aplicaciones,
especialmente en películas finas, catalizadores, pigmentos y transistores.
Palabras clave: nanopartículas; óxido de zinc; Pilas carbono
Zinc.
Abstract
Cells and batteries
are devices in which chemical energy is transformed into electrical energy.
When disposed of, they can pollute the environment; their zinc content in pure
form and in the form of oxides represents an important percentage of the total
weight. In order to take advantage of the carbon zinc batteries, the zinc oxide
nanoparticles were recovered by the alkaline electrolysis method and
characterized in order to know their structural characteristics by means of
scanning electron microscopy (SEM). The distribution of the particles is
variable in the 500 nm scale, it shows crystalline conglomerates constituted by
smaller and elongated particles between 66 and 115 nm that are far from a
characteristic hexagonal symmetry wursite type, nevertheless, the X-Ray
diffraction pattern is similar to the standard pattern for zinc oxide. These
nanoparticles can be used for their higher energy and surface area in multiple
applications; especially in thin films, catalysts, pigments, and transistors.
Keywords: nanoparticles;
zinc oxide; Zinc carbon batteries.
1. Introducción
El mundo avanza a pasos agigantados y con ello el ser
humano cambia sus hábitos y costumbres. No es un secreto que en la actualidad
las personas son muy consumistas y hacen uso constante de aparatos electrónicos
que conllevan al uso continuo de almacenadores de corriente eléctrica. Al
agotarse la energía de estos dispositivos, conocidos como pilas, son
desechadas, ocasionando un daño grave al medio ambiente, debido a sus
componentes tóxicos, los cuales afectan directamente a las aguas subterráneas,
superficiales, flora y fauna. Cada día se desechan miles de millones de pilas
en todo el mundo, la mayoría de las cuales son alcalinas y de zinc-carbono
(Ayala, 2017). Así, los sistemas de contención actuales son inadecuados y los
materiales que componen la batería no pueden ser reutilizados; además, solo
existen programas de devolución basados únicamente en la conciencia social del
consumidor (Castro y Díaz, 2004). En general, los contaminantes, tanto los
líquidos como los gases que generan las pilas, afectan la salud de quienes los
rodean (Agencia de protección Ambiental de Estados Unidos, 2012).
La recuperación y reciclaje de estos materiales es de
suma importancia y en esa dirección diversos estudios han investigado la
recuperación de sus componentes como el zinc (Alvarado et. Al., 2010; Romina,
2013; Medina, 2014; García y Ochoa, 2018) con atractivos rendimientos. La
obtención de zinc en forma de nanopartículas favorece su uso en distintas aplicaciones
como consecuencia de su mayor energía y área superficial, entre otras
propiedades, beneficia su uso en textiles, películas finas, catalizadores,
pigmentos y transistores y transductores (Yadav et al., 2006; Pérez et al.,
2008; Osama et al., 2008; Hingorani et al., 1993). Para su obtención, existe
diversos métodos como la síntesis por precipitación, la síntesis química y la
síntesis por el método hidrotermal (Aquino et al., 2018).
Por tanto, la investigación propone la electrólisis para
la recuperación de óxido de zinc en forma de nanopartículas y su
caracterización a partir de pilas alcalinas de carbono/zinc.
2. Objetivo
Caracterizar las nanopartículas de óxido de zinc
obtenidas a través de la electrólisis de material recuperado de las pilas
alcalinas carbono Zinc.
3. Métodos
3.1.
Recuperación de Zinc
En la primera fase, se recuperó el
zinc y el dióxido de manganeso utilizando el método físico-mecánico de
desmantelamiento. Primero se retiró la carcasa exterior de acero que cubre la
pila, luego se cortó y retiró el envoltorio de plástico que separaba la carcasa
de acero y el zinc; en seguida, se separó el zinc que envolvía al dióxido de
manganeso, finalmente se retiró la barra de carbono.
3.2.
Obtención de nanopartículas de óxido de zinc a través de electrólisis
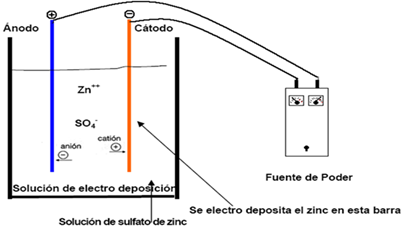
La electrólisis es una etapa de
descomposición química que se produce a través de la fuente que lleva la
corriente e incluye tener un electrólito, que es una sustancia que se puede
cambiar a través de la fuente de la corriente, tal como se observa en la figura
1. Tiene una masa o cuerpo sólido, que puede o no ser un buen conductor, por lo
que se utilizan diferentes tipos de disolventes (Field, S y A Dudley Weill,
1955). En su interior, los aniones liberan electrones (oxidación) en el ánodo y
los cationes atrapan electrones en el cátodo (una reducción).
|
Figura
1 Celda
Electroquímica para obtención de nanopartículas de ZnO |
|
|
|
Nota. Celda Electroquímica para
obtención de nanopartículas de ZnO obtenida de Pérez (2011). |
El electrólito es una solución de medio conductor (H2O
+ NaCl), a través de la cual la corriente se cambia químicamente de acuerdo con
la ley de Faraday, mientras que los electrodos están ubicados, siendo el Zinc
en el Ánodo (+) y Carbono en el Cátodo (-), que reaccionan cuando se alimenta
de energía continúa emitida por fuente de poder. Cuando la solución se coloca
en la batería, la corriente es transportada por iones entre los electrodos. Los
iones o aniones cargados negativamente son atraídos a un electrodo cargado positivamente
y la oxidación ocurre allí (ánodo); en este caso, el catión (+) zinc se oxida
en una solución electrolítica, mientras que la oxidación de los aniones se
reduce oxígeno.
Para la
obtención de nanopartículas, se preparó el electrólito; la cuba fue de 0,75
litros, el área de 48,5 cm2, rectificador de corriente a una
densidad de 0,05 - 0,35 A/cm2, área del ánodo: ancho (5,0 cm) x
altura (9,7 cm) x 2 (dos caras) = 97 cm2, se utilizó 0,02 Amp/cm2
preparándose un electrólito de 270 ml de H20 con 25 g. NaCl (92,6
g/l), se instaló el ánodo (Zinc) y el cátodo (barra de carbono) y, finalmente,
se electrolizó obteniéndose óxido de Zinc. El pH de trabajo fue de 7,52.
En general, las etapas del proceso de obtención de
las nanopartículas se inician después de la recuperación del zinc metálico
aplicando electrólisis alcalina, lavado, secado y obtención de nanopartículas
de zinc.
4. Resultados
La microscopía electrónica de barrido
(SEM) realizada a las nanoparticulas a través de un microscopio electrónico de
barrido de emisión de campo marca Thermoscientific modelo Quattro S, mostrado
en la figura 2, se observa una distribución variable en la escala de medición
de 500 nm que muestra conglomerados
cristalinos (similar al que en la naturaleza se observa a un cúmulo de arroz).
Estos conglomerados cristalinos están constituidos a su vez por partículas más
pequeñas y alargadas entre 66 y 115 nm.
|
Figura
2 Forma estructural de
nanopartículas de óxido de zinc sintetizadas por electrólisis a partir de
pilas recicladas |
|
|
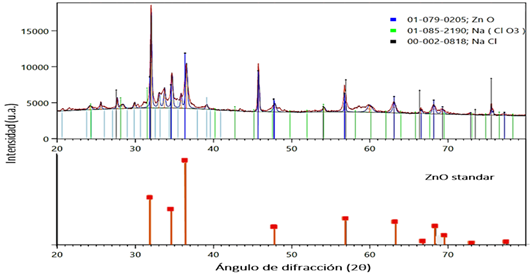
Los
patrones de difracción de rayos X a las nanopartículas mostradas en la figura
3, se determinaron mediante un difractómetro de rayos X, marca PANalytical,
modelo Aeris research, donde se aprecia que existen notoriamente diferentes
picos identificados y asignados a las deflexiones que obedecen al patrón de
difracción estándar para óxido de zinc, además, es similar al obtenido por
Ramírez-Barrón et al. (2019).
|
Figura 3 Patrones de difracción de rayos
X a las nanopartículas obtenidas por electrólisis |
|
|
|
Nota. Las
partículas fueron determinadas en polvo (sin lavar fases presentes Zincita ZnO, Clorato de Sodio
Na(ClO3) y Cloruro de Sodio NaCl. |
La caracterización morfológica de
las nanopartículas sirve para interpretar sus propiedades tanto físicas como
químicas que podrían servir para su empleo para diferentes aplicaciones. Por
ello la determinación de la disfracción de rayos X y el análisis morfológico
resulta importante. Las nanopartículas obtenidas se muestran como conglomerados
cristalinos que están constituidos a su vez por partículas más pequeñas y
alargadas entre 66 y 115 nm, las formas difieren a lo encontrado por Colonia et
al, (2013), quienes obtuvieron conglomerados esféricos entre 100 y 200 nm de
apariencia racimosa al obtener óxido de zinc mediante la ruta sol-gel. Por su
parte, Aquino et al, (2018) encontraron que nanopartículas de óxido de zinc
sintetizadas por el método de precipitación, presentaron una distribución
homogénea con morfología semiexagonal compatible con la naturaleza cristalina
con un tamaño promedio de 90,4 ± 10,6 nm medidos mediante microscopía
electrónica de transmisión (TEM).
La variación del tamaño (66 – 115
nm) no resulta muy precisa principalmente debido a las condiciones de medición
debido a la presencia de impurezas como NaCl, que resulta de no lavar
adecuadamente el compuesto obtenido, pero resulta interesante el sistema
cristalización encontrado que no pertenecen a un sistema cristalino hexagonal
que corresponde a una estructura tipo wurtzita (Aquino et al., 2018), más bien
presentan estructuras alargadas que distan de una simetría hexagonal, siendo en
general una estructura cristalina hemimórfica.
5. Conclusiones
Las nanopartículas de óxido de zinc fueron sintetizadas por electrólisis
alcalina, evidenciando que los tamaños de los cristalitos determinados por
difracción de rayos X, no obstante, se encuentran conglomeradas que muestran
una apariencia de cristales alargados con tamaños entre 66 y 115 nm, que distan
de una simetría hexagonal, el patrón de difracción de rayos X es similar al
patrón estándar para óxido de zinc.
6. Referencias Bibliográficas
Agencia de
Protección Ambiental Estados Unidos.
(2012). Guía Ciudadana de Solidificación y Estabilización. (Artículo, Estados Unidos).
https://cluin.org/download/Citizens/a_citizens_guide_to_solidification_and_stabilization.pdf.
Alvarado, González y Mendoza
(2010). Propuesta de un método para la recuperación de zinc de pilas alcalinas
usadas bajo el enfoque de producción más limpia [Tesis de pregrado, para optar
el Título de Ingeniero Químico de la Universidad El Salvador, Escuela de
Ingeniería Química].
Aquino, Pablo, Osorio, Ana
María, Ninán, Efraín, & Torres, Fernando. (2018). Caracterización de
nanopartículas de ZnO sintetizadas por el método de precipitación y su
evaluación en la incorporación en pinturas esmalte. Revista de la Sociedad
Química del Perú, 84(1), 5-17. http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1810-634X2018000100002&lng=es&tlng=es.
Ayala, C. (2017). Propuesta metodológica para la
recuperación de las pilas alcalinas y zinc –carbono. Escuela de Ingeniería
Industrial, Universidad Pedagógica y Tecnológica de Colombia, Sogambo. https://repositorio.uptc.edu.co/bitstream/001/1952/1/TGT-584.pdfCruz,
Colonia, Roberto, Martínez,
Vanessa C., Solís, José L., & Gómez, Mónica M. (2013). Síntesis de
nanopartículas de ZnO2 empleando ultrasonido: caracterización estructural y
morfológica para aplicaciones bactericidas. Revista de la Sociedad Química del
Perú, 79(2), 126-135, de http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1810-634X2013000200005&lng=es&tlng=es.
Castro, J. y Díaz, M. L. (2004).
La contaminación por pilas y baterías en México. Gaceta Ecológica, (72) pp.
53-74. http://www.redalyc.org/pdf/539/53907205.pd
García y Ochoa (2018). Recuperación de Hidróxido de Zinc, Sulfuro de Manganeso y Oxido de Plata a Partir de Pilas
(Alcalinas D-2, Ácidas
AAA, y pilas de botón). Tesis
de pregrado. Para obtener el título profesional de ingeniero químico. Escuela de ingeniería química.
Universidad nacional de san Agustín
de Arequipa.
Hingorani S, Pillai V, Kumar P, Multani MS, Shah DO
(1993). Síntesis
mediada por microemulsión de nanopartículas de óxido de zinc para estudios de
varistores. Mat Res Bull. 28: 1303-1310. https://www.sciencedirect.com/science/article/abs/pii/002554089390178G
Medina, (2014). Influencia de
relación materia primaria / solvente en la extracción de manganeso de pilas
alcalinas utilizando ácido acético y ácido cítrico [Tesis de Pregrado, para
optar el Título de Ingeniero Ambiental, Escuela de Ingeniería Ambiental,
Universidad Nacional de Trujillo].
http://dspace.unitru.edu.pe/bitstream/handle/UNITRU/3237/MedinaLLerena_J.pdf?sequence=1&isAllowed=y
Osama M, El Fekya, Hassanb EA,
Fadelb SM, Hassanb ML. (2014). Uso de nanopartículas
de ZnO para la protección de pinturas al óleo sobre soporte de papel contra la
suciedad, el ataque de hongos y el envejecimiento por UV. J Cult Herit. 2014; 15: 165-172. https://www.sciencedirect.com/science/article/abs/pii/S1296207413000642
Pérez, J. A. P., Gallego, J. L.,
Roman, W. S., & Landázuri, H. R. (2008). Películas nanoestructuradas de
óxido de zinc (ZnO). Scientia et
technica, 14(39), 416-421. https://www.redalyc.org/pdf/849/84920503076.pdf
Pérez,
J. (2011). Obtención de polvos de zinc
por vía electrolítica.
https://bibliotecadigital.univalle.edu.co/handle/10893/4720
Romina, M. (2013). Optimización
de un proceso biohidrometalúrgico de recuperación de metalesde pilas alcalinas
y de cinc-carbón agotadas [Tesis Doctoral, Facultad de Ciencias Exactas,
Universidad de la Plata, Argentina]. http://sedici.unlp.edu.ar/bitstream/handle/10915/29548/Documento_completo__.pdf?sequence=1&isAllowed=y
Yadav A, Prasad V, Kathe AA, Raj
S, Yadav D, et al. (2006). Acabado funcional en tejidos de algodón utilizando
nanopartículas de óxido de zinc. Bull Mater Sci. 29: 641–645. https://doi.org/10.1007/s12034-006-0017-y